Il permanganato di potassio, a detta degli esperti dell'ARPA, è del tutto innoquo. e probabilmente lo è, visto che la tossicità di una sostanza è sempre proporzionale alla dose.
Stando a quanto racconta Wikipedia però la sostanza non é del tutto inerte.... a voi la sentenza.
Da Wikipedia, l'enciclopedia libera.
| Permanganato di potassio | |
|---|---|
 | |
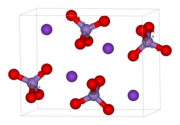 | |
| Nome IUPAC | |
| tetraossomanganato (VII) di potassio | |
| Caratteristiche generali | |
| Formula bruta omolecolare | KMnO4 |
| Peso formula (u) | 158,04 |
| Aspetto | solido cristallino violetto |
| Numero CAS | [] |
| Numero EINECS | 231-760-3 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, inc.s.) | 2,70 |
| Solubilità in acqua | 64 g/l a 293 K |
| Temperatura di fusione (K) | >510 (>240 °C) con decomposizione |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | -837,2 |
| ΔfG0 (kJ·mol−1) | -737,6 |
| S0m(J·K−1mol−1) | 171,7 |
| C0p,m(J·K−1mol−1) | 117,6 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
pericolo
| |
| Frasi H | 272 - 302 - 410 |
| Consigli P | 210 - 273 [1] |
Il permanganato di potassio (o potassio permanganato, nome IUPAC tetraossomanganato (VII) di potassio) è il sale di potassio dell'acido permanganico, derivato dal manganese. La sua formula bruta è KMnO4 ed il suo numero CAS è 7722-64-7.
Puro, si presenta come un solido cristallino dal tipico colore viola scuro. È solubile in acqua (64 g/l a 20 °C); meno lo è anche in etanolo, ma la soluzione non è stabile perché il permanganato di potassio ossida l'etanolo, decomponendosi.
È stato scoperto nel 1659; viene utilizzato come comburente in alcune composizioni per uso pirotecnico e - in soluzione diluita - come agente disinfettante e deodorante, come collutorio, come antiparassitario per i pesci e come antidoto all'avvelenamento da fosforo. Viene anche utilizzato per la raffinazione dellacocaina. Agli albori della fotografia era un componente della polvere per le lampade flash.
L'importanza del permanganato di potassio in chimica analitica è proprio dovuta al suo essere un potente agente ossidante. In ambiente acido lo ionepermanganato MnO4- è in grado di ossidare molti composti riducendosi a ione Mn2+. Un esempio particolarmente noto e importante consiste nella determinazione dell'ossidabilità secondo Kubel di un campione di acqua.
Essendo inoltre lo ione permanganato di colore violetto scuro e lo ione Mn2+ incolore, l'uso di una soluzione acquosa di permanganato di potassio per condurre una titolazione di ossido-riduzione rende superfluo l'uso di un indicatore.
Si consiglia di maneggiare questo sale e le sue soluzioni indossando un paio di guanti di lattice. Non solo per via della sua tossicità, ma anche perché a contatto con la pelle lascia persistenti macchie scure di biossido di manganese, che possono essere tolte strofinando con soluzione acidulata diluita di solfito obisolfito sodico.
Il permanganato di potassio deve essere conservato al riparo dalla luce (si usano abitualmente bottiglie di vetro ambrato) e privo di umidità.

Nessun commento:
Posta un commento